POCUS NEL CONTESTO PREOPERATORIO – CUORE
Fabio Magarotto1, Federica Arturi1, Gabriele Melegari2
- Università degli Studi di Modena e Reggio Emilia, Scuola di Specializzazione Anestesia e Rianimazione, Terapia Intensiva e del Dolore
- Azienda Ospedaliero Universitaria Policlinico di Modena, Anestesia e Rianimazione II servizio
Un approccio clinico moderno e aggiornato all’anestesia integra sempre più l’utilizzo dell’ecografo, uno strumento versatile che trova applicazione in numerosi ambiti. Tra questi, negli ultimi anni, si è affermata in particolare la tecnica POCUS: una valutazione ecografica mirata a specifici quesiti clinici, capace di offrire un inquadramento più dettagliato e integrato rispetto al solo esame obiettivo tradizionale. Non a caso, l’ecografo viene spesso descritto come uno “stetoscopio di secondo livello”. 1,2
Ricordiamo che i vantaggi della tecnica POCUS (Point Of Care UltraSound) sono:
- Costo ridotto, in quanto è sufficiente disporre di un ecografo con le sonde adeguate
- Rapidità, poiché è una valutazione veloce e che risponde a quesiti clinici specifici (a differenza di una valutazione specialistica completa che richiede tempo e organizzazione)
- Immediatezza, infatti nasce come tecnica da applicare al letto del paziente nel contesto di cura e in tempo reale
- Può essere praticata anche da personale non specialistico dato che la curva di apprendimento è accessibile
Al contempo, è sempre opportuno tenere presente le limitazioni legate alla metodica ecografica3:
- È una tecnica operatore dipendente, sono necessarie formazione ed esperienza per un buon livello di precisione e di affidabilità
- È necessaria la disponibilità dei dispositivi, talvolta condivisi tra tanti operatori (per esempio in un blocco operatorio con numerose sale e un solo ecografo a disposizione)
- Consente la valutazione di un momento “specifico” in termini di tempo, e per questo motivo non è la scelta ideale per eseguire un monitoraggio costante.
- Accesso al paziente, che può essere limitato nel contesto intraoperatorio o se vi sono medicazioni. Inoltre, il paziente può trovarsi in decubito obbligato rendendo difficile una buona visione da alcune finestre cosi come la presenza di alcune variabilità anatomiche può non garantire una riuscita ottimale dell’esame.
- Alcuni dati raccolti con l’ecografia possono darci un senso di falsa sicurezza; le informazioni che otteniamo devono sempre essere integrate nel contesto clinico e anamnestico del paziente
Nel contesto preoperatorio si verificano spesso tempi di attesa (per esempio l’attesa del tempo di azione dell’anestetico locale dopo aver fatto un blocco nervoso), che possono costituire un’occasione per fare una valutazione ecografica e raccogliere informazioni potenzialmente utili nella gestione clinica anestesiologica4,5.
La valutazione ecografica come integrazione della valutazione tradizionale non richiede molto tempo e può migliorare la nostra consapevolezza del quadro clinico del paziente. Esistono diversi impieghi per questa tecnica nel contesto perioperatorio (cuore, polmoni, vie aeree difficili, stomaco, addome ecc.)6–8. Uno degli apparati di maggiore interesse per l’anestesista è sicuramente quello cardiovascolare.
Il POCUS cardiaco permette una valutazione in tempo reale di contrattilità cardiaca, presenza di versamento, disfunzioni valvolari rilevanti e grossi vasi, con la possibilità di trarre alcuni dati sullo stato emodinamico del paziente. È utile vedere il POCUS cardiaco come un’estensione dell’esame obiettivo per poter rilevare segni di scompenso cardiaco o di instabilità emodinamica9.
In ambito non specialistico ci si avvale spesso di una valutazione “eye-balling” di tipo qualitativo (ovvero “a colpo d’occhio”, pratica legittimata anche dalla letteratura se praticata da personale che ha acquisito sufficiente esperienza10) e di poche misurazioni quantitative.
Il POCUS cardiaco preoperatorio può trovare applicazione nel contesto dell’urgenza, quando manca il tempo per organizzare una valutazione specialistica completa, mentre in elezione trova impiego dove la valutazione approfondita cardiologica non avrebbe una indicazione vera e propria. Come sappiamo, le indicazioni a una valutazione ecocardiografica ambulatoriale completa sono relativamente ristrette (pazienti sintomatici per scompenso cardiaco, scarsa tolleranza allo sforzo fisico, sospetta insorgenza di patologie cardiovascolari o patologie importanti non controllate negli ultimi 90 giorni, dispnea ad eziologia sconosciuta, riscontro di un soffio cardiaco non noto)11,12. Si è infatti osservato che una quota significativa di valutazioni specialistiche preoperatorie non rispondano a tutti i criteri di appropriatezza, specialmente i casi inviati come semplice controllo di cardiopatia ischemica cronica nota clinicamente stabile e ipertensione non complicata13.
Non sono state codificate indicazioni precise per la scelta di quali pazienti sottoporre a POCUS cardiaco. La scelta è valutabile caso per caso e dipende da indicazione anestesiologica a seconda delle tempistiche a disposizione, delle informazioni che si cerca di ottenere e di conseguenza se è possibile garantire maggiore sicurezza al paziente adeguando la pratica clinica14.
Un esempio di potenziale paziente dove una valutazione POCUS può essere utile è un caso di frattura di femore in paziente anziano senza una anamnesi cardiologica nota, in cui sapere se presenta una stenosi aortica o una disfunzione ventricolare possono permettere all’anestesista di adottare una strategia anestesiologica appropriata.
L’obiettivo della valutazione POCUS è quello di avere una risposta più o meno autonoma ad alcuni quesiti clinici, come una sorta di test di screening, pur tenendo presente che il compito dell’anestesista non è quello di sostituirsi al cardiologo o al radiologo nell’esecuzione di un esame diagnostico completo, ma è quello di acquisire maggiore consapevolezza sulle condizioni cliniche del paziente per migliorare la qualità dell’esame obiettivo con tutti gli strumenti a propria disposizione.
Le domande a cui si tenta di rispondere con una valutazione ecocardiografica puramente qualitativa sono:
- Il ventricolo sinistro appare significativamente dilatato?
- La funzionalità contrattile del ventricolo sinistro appare grossolanamente anomala?
- Il ventricolo destro appare dilatato?
- Il paziente ha un ritorno venoso insufficiente?
- Sono presenti patologie valvolari significative?
- È presente versamento pericardico?
- La vena cava inferiore è collassabile?
A livello preoperatorio le informazioni che possiamo ottenere con questo esame possono modificare il profilo di rischio perioperatorio mediante:
- La scelta di inviare il paziente a un controllo specialistico avanzato
- L’ottimizzazione della terapia medica
- La scelta della tecnica anestesiologica o chirurgica
- Il livello di monitoraggio intraoperatorio
- Il livello di intensità di cure nel postoperatorio
Prendere confidenza con la valutazione ecografica permette anche all’anestesista di interfacciarsi con colleghi specialisti con una maggiore quantità di informazioni, favorendo un dialogo più immediato e un inquadramento clinico più rapido e preciso.
A livello intra e postoperatorio invece il POCUS cardiaco è più applicabile nel diagnosticare le complicanze o per mantenere una sorta di monitoraggio emodinamico15, per riconoscere e inquadrare ipovolemia, ipotensione non spiegata, disfunzioni ventricolari, sospetto di ischemia e alterazioni ECG di nuova insorgenza.
Ricordiamo che con l’ecografia transtoracica è difficile ottenere un vero e proprio monitoraggio emodinamico intraoperatorio a differenza della ecocardiografia transesofagea, che tuttavia costituisce un argomento degno di trattazione dedicata separatamente.
Alcuni studi mostrano come l’integrazione nella pratica clinica di protocolli con POCUS cardiaco possa cambiare le scelte compiute sulla gestione clinica e portare a un outcome migliore16–18.
POCUS CARDIACO19,20
Alcuni cenni sulla tecnica ecografica per eseguire un’ecografia cardiaca transtoracica:
- La sonda utilizzata è la sonda Sector, tipicamente una phased array
- I movimenti della sonda da attuare per ottimizzare le immagini sono di traslazione, rotazione e tilting
- Il marker della sonda solitamente corrisponde al lato destro dell’immagine visibile sullo schermo
- Il guadagno deve essere settato perché il sangue presente all’interno delle cavità cardiache appaia di colore nero
- La profondità va adattata e contestualizzata alla proiezione, idealmente deve comprendere solamente le strutture di interesse al fine di minimizzare la latenza e la definizione dell’immagine.
- La modalità più utilizzata per le immagini è la modalità B-Mode. Per ottenere dati quantitativi ci si avvale anche di altre modalità come M-Mode, Color-Doppler e Doppler continuo (Continuous Wave Doppler, CW) o pulsato (Pulsed Wave Doppler, PW)
- Le strutture anatomiche in immagine sono generalmente osservate partendo da ore 12 e procedendo in senso orario
- Le tre finestre generalmente utilizzate per l’ecocardiografia transtoracica sono parasternale, apicale e sottocostale
- In ciascuna proiezione si valutano informazioni specifiche e peculiari di quella proiezione
FINESTRA PARASTERNALE
La visione ottimale da questa finestra è ottenuta con il paziente in posizione laterale sinistra e a bassi volumi polmonari (a fine espirazione). Nel paziente supino è comunque solitamente possibile ottenere una visione di qualità accettabile.
Parasternale asse lungo (PLAX)
Piano di scansione parallelo all’asse lungo del ventricolo sinistro, che interseca l’apice del ventricolo sinistro, il centro della valvola aortica, e il centro della valvola mitrale in senso antero-posteriore
Posizione della sonda
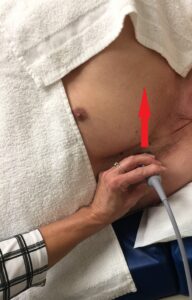
La sonda deve essere posizionata lungo la linea parasternale sinistra con il marker rivolto verso la spalla destra del paziente, e scorrendo tra i vari spazi intercostali (generalmente tra il terzo e il quinto) si trova la finestra che garantisce la migliore visione.
In questa visione è possibile vedere parte del ventricolo destro, la valvola aortica e l’aorta ascendente prossimale, l’atrio sinistro, la valvola mitrale e le pareti anterosettali e inferolaterali del ventricolo sinistro.
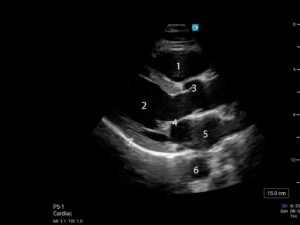
- Ventricolo destro
- Ventricolo sinistro
- Valvola aortica / radice dell’aorta ascendente
- Valvola mitrale
- Atrio sinistro
- Aorta Discendente
- Pericardio
Si valutano
- Ventricolo destro: questa finestra non è la migliore per la valutazione delle dimensioni o della funzionalità del ventricolo destro, ma è possibile notare marcate dilatazioni o disfunzioni di parete. Normalmente la porzione di ventricolo destro osservabile da questa finestra ha dimensioni comparabili a quelle della radice aortica.
- Valvola aortica: una stenosi valvolare è improbabile se la valvola si apre completamente e rapidamente.
- Atrio sinistro: se dilatato e notevolmente più grande rispetto al diametro della radice dell’aorta suggerisce una possibile storia di pressioni atriali sinistre elevate come da disfunzione diastolica, malattie valvolari mitraliche o fibrillazione atriale.
- Valvola mitrale: dovrebbe aprirsi rapidamente in diastole e chiudersi completamente in sistole. Se i lembi della valvola mitrale superano l’anulus mitralico durante la sistole possono indicare prolasso o ribaltamento della valvola mitralica con insufficienza valvolare. Se il lembo anteriore della valvola mitrale non si apre rapidamente, avvicinandosi alla parete anterosettale del ventricolo in diastole, si potrebbe pensare a stenosi valvolare. Lembi valvolari rigidi durante l’apertura possono indicare malattia reumatica valvolare. Un’altra anomalia osservabile in questa visione è un eccessivo movimento anteriore del lembo anteriore della mitrale durante la sistole, che potrebbe indicare un problema di ostruzione dinamica del tratto di efflusso del ventricolo sinistro (LVOT, ovvero il tratto di ventricolo che precede immediatamente la valvola aortica), reperto comune nei pazienti con cardiomiopatia ipertrofica o in pazienti con ventricolo sinistro piccolo e spesso o tessuto valvolare in eccesso; in questi casi, come per ogni difetto valvolare di entità rilevante, si raccomanda una valutazione specialistica.
- Si può avere una valutazione globale del ventricolo sinistro in questa visione nonostante siano osservabili direttamente solo la porzione anterosettale e inferolaterale della parete ventricolare. Inizialmente si può valutare la morfologia del ventricolo, per esempio se la camera appare dilatata o se il tessuto miocardico è ipertrofico. Dopodiché si può valutare la contrattilità: il miocardio si dovrebbe contrarre (ispessimento della parete e avvicinamento di apice e base del ventricolo) rapidamente in sistole. Altri segni qualitativi di buona funzionalità ventricolare includono l’oscillazione antero-posteriore della radice dell’aorta (anteriormente con il riempimento atriale e posteriormente con lo svuotamento atriale) e buona escursione del lembo mitralico anteriore.
- In questa finestra è talvolta possibile osservare la presenza di versamento pericardico, che è eventualmente osservabile come una zona anecogena compresa tra il cuore e l’aorta discendente toracica.
Per approfondimenti che meritano trattazione dedicata rispetto ai concetti base, si richiama inoltre l’attenzione su alcuni metodi semiquantitativi utili per stimare la funzionalità del ventricolo sinistro, come la Shortening Fraction (SF) (un indice lineare della funzione sistolica ventricolare che esprime in percentuale l’accorciamento del diametro telediastolico del ventricolo fra diastole e sistole misurabile tramite M-mode) e il confronto tra l’area telediastolica e area telesistolica, la cui riduzione in percentuale normale riflette una contrattilità ventricolare non alterata.
Un ulteriore importante vantaggio, grazie all’introduzione di applicazioni di intelligenza artificiale e di sistemi di automatizzazione nelle nuove macchine da ecocardiografia, sarà la possibilità di ottenere stime quantitative della frazione di eiezione (FE) e della funzione ventricolare in modo automatizzato.
Parasternale asse corto (PSAX)
Piano di scansione perpendicolare all’asse lungo del ventricolo sinistro, che mostra una sezione trasversale di entrambi i ventricoli. È possibile ottenere questa scansione a diverse altezze, quella più usata nella tecnica POCUS è a livello dei muscoli papillari (circa a metà altezza del ventricolo), ma spostandosi cranialmente è possibile visualizzare anche le tre cuspidi della valvola aortica.
Posizione della sonda
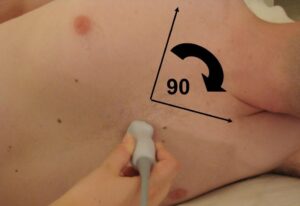
Mantenendo la sonda sulla finestra parasternale per la visione dell’asse lungo, questa visione è ottenuta ruotando la sonda di circa 90° fino a puntare l’indicatore verso la spalla sinistra del paziente.
Prendendo in considerazione la porzione anteriore, laterale, inferiore e settale del cuore, in questa proiezione sono apprezzabili segmenti di tutti i territori di irrorazione delle arterie coronarie destra e sinistra (che si divide in discendente anteriore e circonflessa)
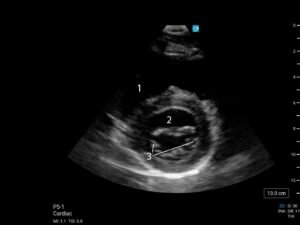
- Ventricolo destro
- Ventricolo sinistro
- Muscoli papillari
L’asse corto parasternale fornisce informazioni importanti sulla funzionalità globale e regionale del ventricolo e sul suo riempimento:
- In condizioni normali i vari segmenti delle pareti del ventricolo sinistro si ispessiscono tutte allo stesso modo durante la sistole. Ispessimento ridotto o assente possono indicare ischemia o infarto coronarico. Tipicamente la coronaria discendente anteriore irrora la porzione anteriore, la circonflessa la porzione laterale e la coronaria destra la porzione posteriore del cuore. In condizioni di ridotto ritorno venoso il ventricolo sinistro si presenta piccolo, scarsamente riempito e ipercinetico, mentre un ventricolo pieno in diastole e che si svuota completamente in sistole può suggerire uno stato di alta portata cardiaca. Questa visione è solitamente utilizzata per fare una stima spannometrica di quanto possa essere la frazione di eiezione del ventricolo sinistro.
- Il ventricolo destro non è valutato idealmente da questa finestra, ma se si presenta di dimensioni notevolmente maggiori rispetto al sinistro può suggerire anomalie del circolo polmonare. Sovraccarichi di pressione o di volume del ventricolo destro possono determinare alterazioni del movimento del setto interventricolare.
- Il setto interventricolare normalmente appare convesso verso il ventricolo destro, in quanto le pressioni nel ventricolo sinistro sono maggiori di quelle nel ventricolo destro in condizioni fisiologiche. Se il setto appare piatto in diastole può indicare uno stato di sovraccarico di volume del ventricolo destro), mentre se il setto appare piatto sia in diastole che in sistole, può indicare una condizione di severa ipertensione polmonare.
- Anche in questa visione è possibile talvolta apprezzare versamento pericardico come una zona anecogena anteriormente al miocardio.
FINESTRA APICALE
La visione ottimale attraverso la finestra apicale si ottiene solitamente nel paziente in decubito parziale laterale sinistro e a bassi volumi polmonari.
Apicale 4 camere (A4C)
Piano di scansione che interseca l’apice cardiaco e le valvole atrio-ventricolari, mostrando entrambi i ventricoli e gli atri.
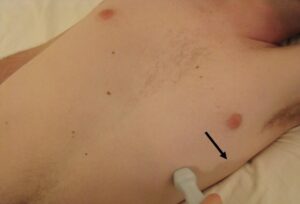
Posizione della sonda
La finestra si trova generalmente a livello del quarto o quinto spazio intercostale tra la linea emiclaveare sinistra e la linea ascellare anteriore sinistra, tuttavia, vi è ampia variabilità anatomica individuale sia in senso medio-laterale che cranio-caudale. L’indicatore della sonda è diretto verso il cavo ascellare sinistro del paziente. Il fascio ultrasonoro viene quindi diretto cranialmente verso la testa del paziente e la sonda viene ruotata fino a posizionare il marker orientativamente alle ore 3.
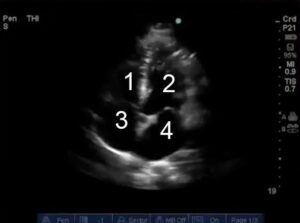
- Ventricolo destro
- Ventricolo sinistro
- Atrio destro
- Atrio sinistro
L’apice del ventricolo sinistro dovrebbe essere al vertice dello schermo, con il setto interventricolare disposto verticalmente al centro dello schermo. Si osservano sulla destra dello schermo le sezioni sinistre del cuore e viceversa. Il ventricolo sinistro è attraversato dal piano di visione nelle sue porzioni inferosettale e anterolaterale. Alla giunzione atrioventricolare si osservano medialmente il lembo anteriore della valvola mitrale e lateralmente il lembo posteriore. È visibile anche il ventricolo destro con la valvola tricuspide, solitamente più vicina all’apice cardiaco rispetto alla valvola mitrale. Gli atri sono visibili nella parte bassa dell’immagine.
Da questa immagine è possibile valutare:
- Ventricolo sinistro: questa finestra è una delle migliori per la valutazione del ventricolo sinistro. Un ventricolo normofunzionante ha un ispessimento simmetrico della parete in sistole, con chiusura pronta della valvola mitrale e un suo rapido avvicinamento all’apice cardiaco e pronta apertura valvola aortica sistolica. Un infarto della arteria coronarica discendente anteriore è ben apprezzabile in questa visione, comportando discinesie del segmento apicale del ventricolo.
- Valvola mitrale: i lembi di una mitrale normale dovrebbero rimanere sotto all’anulus mitralico con adeguata chiusura in sistole. Un prolasso o ribaltamento significativo o una netta mancata chiusura della valvola dovrebbero allarmare in merito a una possibile insufficienza mitralica. Si possono osservare anche calcificazioni o alterazioni reumatiche della valvola.
- Atri: normalmente sono simili in dimensioni tra di loro, e ridotti rispetto ai ventricoli.
- Valvola tricuspide: ben visibile da questa finestra, normalmente si apre interamente in diastole e rimane confinata all’anulus con buona chiusura in sistole. Il prolasso dei lembi valvolari o una chiusura incompleta possono indicare insufficienza mitralica.
Ventricolo destro: questa è la visione ottimale per la valutazione della funzionalità del ventricolo destro, che normalmente dovrebbe apparire più piccolo del sinistro e convergere leggermente sotto all’apice cardiaco. Se all’apice cardiaco i ventricoli appaiono simmetrici e
- le dimensioni del ventricolo destro sono uguali o superiori a quelle del sinistro è lecito sospettare una dilatazione ventricolare destra. Segni di buona contrazione del ventricolo destro sono dati dall’ispessimento della parete libera e dal rapido avvicinamento della valvola tricuspide all’apice cardiaco. Inoltre è possibile calcolare un TAPSE (Tricuspid Annular Plane Systolic Excursion), un parametro affidabile della funzione sistolica del ventricolo destro. Il TAPSE si ottiene tramite l’utilizzo dell’ M-mode orientato sull’anulus tricuspidalico. I suoi valori normali nell’adulto sono generalmente superiori ai 15-16 mm.
Apicale 5 camere (A5C)
Simile alla visione apicale quattro camere, ma include anche la radice aortica con la valvola aortica.
Posizione della sonda
Questa visione è ottenuta partendo dalla visione apicale quattro camere, con un tilting maggiore della sonda in senso craniale in modo da visualizzare la radice della aorta con la valvola aortica.
Viene utilizzata principalmente per il calcolo dell’integrale velocità-tempo (VTI), che integrato ad altri dati quali il diametro del tratto di deflusso del ventricolo sinistro (LVOT – Left Ventricular Outflow Tract) acquisito in parasternale asse lungo per il calcolo dell’area LVOT che permette di stimare la gittata sistolica e il cardiac output se moltiplicato per la frequenza cardiaca FC.
FINESTRA SOTTOCOSTALE
Le immagini migliori da questa finestra sono ottenute con il paziente in posizione supina, ad alti volumi polmonari. L’abbassamento del diaframma avvicina il cuore alla sonda.
Sottocostale 4 camere (S4C)
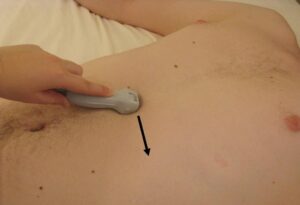
Posizione della sonda
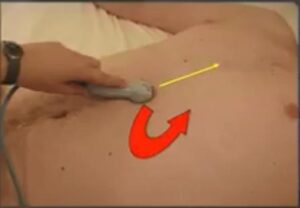
Si trova generalmente un paio di centimetri sotto al processo xifoideo dello sterno. Per ottenere le immagini migliori ci si avvale del fegato per la sua ecogenicità, piuttosto che dello stomaco; la sonda, quindi, va mantenuta a livello mediano se non leggermente alla destra del paziente, con l’indicatore della sonda rivolto alla sinistra del paziente. Applicare pressione per affondare la sonda al di sotto del livello dello sterno può migliorare la visione.
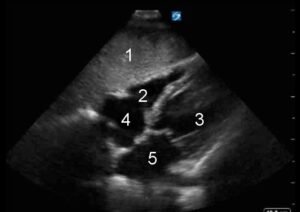
- Parenchima epatico
- Ventricolo destro
- Ventricolo sinistro
- Atrio destro
- Atrio sinistro
Da questa finestra appare una sezione più bassa del ventricolo destro rispetto all’apicale quattro camere, con una visione del ventricolo sinistro meno informativa rispetto alle finestre precedentemente elencate
Da questa finestra è ben visibile la parete libera del ventricolo destro, complementando così le informazioni ottenute dalle altre finestre. È comunque possibile una valutazione globale anche da questa finestra, nel caso in cui le altre finestre siano scarsamente accessibili.
Il ventricolo destro deve normalmente avere dimensioni inferiori rispetto al sinistro. Da questa finestra le dimensioni del ventricolo destro sono tuttavia generalmente sottostimate.
Questa finestra è anche ottimale per la valutazione del versamento pericardico, osservabile quando il cuore è circondato da uno spazio anecogeno. Il tamponamento cardiaco può manifestarsi con inversione dell’atrio destro durante la sistole, compressione del ventricolo destro durante la diastole e dilatazione della vena cava inferiore. Inoltre è una finestra che può essere utilizzata per valutare la qualità delle compressioni toraciche in corso di rianimazione cardiopolmonare.
Sottocostale vena cava inferiore
Posizione della sonda
Partendo dalla visione sottocostale quattro camere, centrando l’atrio e ruotando la sonda fino a puntare il marker verso la testa del paziente si dovrebbe ottenere l’immagine della VCI che si abbocca nell’atrio destro.
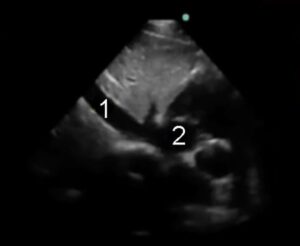
- Vena cava inferiore
- Atrio destro
Nella parte superiore dell’immagine si osserva il parenchima epatico, sovrastante alla VCI visibile in orizzontale mentre entra nell’atrio di destra. La vena epatica che si immette nella VCI è frequentemente visibile a breve distanza dall’atrio destro, sopra alla VCI. È importante fare attenzione a non confondere la VCI con l’aorta, che solitamente ha una parete più spessa e una chiara attività pulsatile.
La valutazione delle dimensioni della VCI è generalmente usata come indice di stato volemico e predittore di fluid responsiveness21. Una VCI dilatata è suggestiva di elevate pressioni venose centrali e indica minori probabilità di fluid responsiveness. Una VCI piccola e collabente è spesso osservabile in pazienti in condizioni di fluid responsiveness. Si tenga in mente che la valutazione dello stato volemico è un aspetto molto complesso, le informazioni raccolte mediante ecografia devono essere integrate nel contesto clinico e non prese da sole.
Immagini gentilmente concesse da Sonosite Fujifilm
- Lenk T, Whittle J, Miller TE, Williams DGA, Bronshteyn YS. Focused cardiac ultrasound in preoperative assessment: the perioperative provider’s new stethoscope? Perioper Med (Lond). 2019;8:16. doi:10.1186/s13741-019-0129-8
- Li L, Yong RJ, Kaye AD, Urman RD. Perioperative Point of Care Ultrasound (POCUS) for Anesthesiologists: an Overview. Current Pain and Headache Reports. Published online 2020. doi:10.1007/s11916-020-0847-0
- Gohad R, Jain S. The Use of Point-of-Care Ultrasound (POCUS) in Anesthesiology: A Narrative Review. Cureus. 16(9):e70039. doi:10.7759/cureus.70039
- McCormick TJ, Miller EC, Chen R, Naik VN. Acquiring and maintaining point-of-care ultrasound (POCUS) competence for anesthesiologists. Can J Anesth/J Can Anesth. 2018;65(4):427-436. doi:10.1007/s12630-018-1049-7
- Meier I, Vogt AP, Meineri M, Kaiser HA, Et. A. Point-of-care ultrasound in the preoperative setting. Best Practice & Research Clinical Anaesthesiology. Published online 2020. doi:10.1016/j.bpa.2020.04.010
- Segura-Grau E, Antunes P, Magalhães J, Vieira I, Segura-Grau A. Minute Zero: an essential assessment in peri-operative ultrasound for anaesthesia. Anaesthesiol Intensive Ther. 2022;54(1):80-84. doi:10.5114/ait.2022.112886
- Kalagara H, Coker B, Gerstein NS, et al. Point-of-Care Ultrasound (POCUS) for the Cardiothoracic Anesthesiologist. Journal of Cardiothoracic and Vascular Anesthesia. 2022;36(4):1132-1147. doi:10.1053/j.jvca.2021.01.018
- Arumugam S, Kolli S, Brakoniecki K, Singh PA, Kukreja P, Kalagara H. Point-of-care Ultrasound (POCUS) for the Regional Anesthesiologist. Curr Anesthesiol Rep. 2024;14(2):231-248. doi:10.1007/s40140-024-00622-3
- Noor A, Liu M, Jarman A, Yamanaka T, Kaul M. Point-of-Care Ultrasound Use in Hemodynamic Assessment. Biomedicines. 2025;13(6):1426. doi:10.3390/biomedicines13061426
- Gudmundsson P, Rydberg E, Winter R, Willenheimer R. Visually estimated left ventricular ejection fraction by echocardiography is closely correlated with formal quantitative methods. International Journal of Cardiology. 2005;101(2):209-212. doi:10.1016/j.ijcard.2004.03.027
- Halvorsen S, Mehilli J, Cassese S, et al. 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery: Developed by the task force for cardiovascular assessment and management of patients undergoing non-cardiac surgery of the European Society of Cardiology (ESC) Endorsed by the European Society of Anaesthesiology and Intensive Care (ESAIC). Eur Heart J. 2022;43(39):3826-3924. doi:10.1093/eurheartj/ehac270
- Thompson A, Fleischmann KE, Smilowitz NR, et al. 2024 AHA/ACC/ACS/ASNC/HRS/SCA/SCCT/SCMR/SVM Guideline for Perioperative Cardiovascular Management for Noncardiac Surgery: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2024;150(19):e351-e442. doi:10.1161/CIR.0000000000001285
- Tank A, Hughey R, Ward RP, Nagele P, Rubin DS. Evaluation of Appropriate Use of Preoperative Echocardiography Before Major Abdominal Surgery: A Retrospective Cohort Study. Anesthesiology. 2021;135(5):854-863. doi:10.1097/ALN.0000000000003984
- Sabogal RC. Exploring the Applicability of Pre-Anesthetic Cardiac POCUS in Unexpected Conditions: Could it be Helpful? POCUS J. 8(2):237-242. doi:10.24908/pocus.v8i2.16519
- Poelaert J, Malbrain M. Cardiac ultrasound: a true haemodynamic monitor? Anaesthesiology Intensive Therapy. 2019;50(4). Accessed March 8, 2026. https://www.termedia.pl/Cardiac-ultrasound-a-true-haemodynamic-monitor-,118,38017,0,1.html
- Canty DJ, Heiberg J, Yang Y, et al. Pilot multi-centre randomised trial of the impact of pre-operative focused cardiac ultrasound on mortality and morbidity in patients having surgery for femoral neck fractures (ECHONOF-2 pilot). Anaesthesia. 2018;73(4):428-437. doi:10.1111/anae.14130
- Deswal S, Yadav S, jakhar A, Sheoran M, Chauhan P, Mishra J. Preoperative cardiac POCUS in high-risk non-cardiac surgery: A prospective study on anesthetic planning and outcomes. Bioinformation. 2025;21(10):3784-3787. doi:10.6026/973206300213784
- Sheth A, Dabo-Trubelja A. Perioperative focused cardiac ultrasound: a brief report. J Anesth Crit Care. 2021;13(1):55-60.
- Zimmerman JM, Coker BJ. The Nuts and Bolts of Performing Focused Cardiovascular Ultrasound (FoCUS). Anesthesia & Analgesia. 2017;124(3):753-760. doi:10.1213/ANE.0000000000001861
- Mitchell C, Rahko PS, Blauwet LA, et al. Guidelines for Performing a Comprehensive Transthoracic Echocardiographic Examination in Adults: Recommendations from the American Society of Echocardiography. Journal of the American Society of Echocardiography. 2019;32(1):1-64. doi:10.1016/j.echo.2018.06.004
- Caplan M, Durand A, Bortolotti P, et al. Measurement site of inferior vena cava diameter affects the accuracy with which fluid responsiveness can be predicted in spontaneously breathing patients: a post hoc analysis of two prospective cohorts. Ann Intensive Care. 2020;10:168. doi:10.1186/s13613-020-00786-1
